Droitcourt C et al. Safety of oral Propranolol for infantile hemangioma. Pediatrics, 2018;141:e20173783.
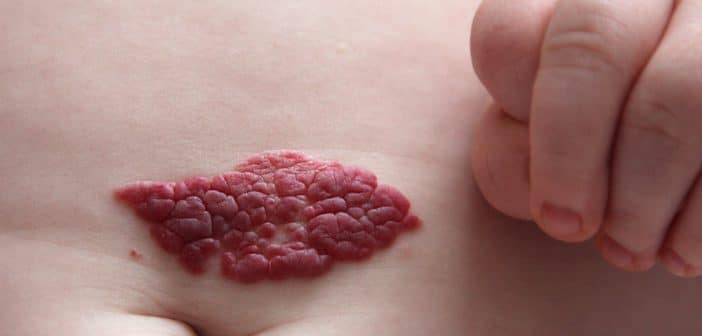
Les hémangiomes infantiles sont des tumeurs des tissus mous dont la prévalence précise n’est pas connue mais estimée à 4-5 % chez les enfants de race blanche. L’évolution naturelle comprend 3 phases cliniques. Ces tumeurs apparaissent dans les jours ou semaines après la naissance puis ont une phase de croissance jusqu’à 6 mois, suivie d’une phase de stabilisation jusqu’à 12-18 mois et enfin une phase d’involution progressive. Une régression complète est observée dans plus de 80 % des cas à 4 ans. Cependant, un traitement est parfois nécessaire pour éviter ou traiter une complication. En 2008, un essai randomisé français en double aveugle a confirmé l’efficacité et la tolérance du propranolol oral à la dose de 3 mg/kg/j. En 2014, le traitement a été approuvé par l’agence européenne du médicament. Depuis cette date, plusieurs effets secondaires graves, cardiovasculaires, respiratoires et métaboliques ont été rapportés mais il est parfois difficile de différencier ces effets des complications liées à l’hémangiome ou aux syndromes parfois associés à ceux-ci.
L’objectif de l’étude était d’évaluer la sécurité d’utilisation du propranolol oral à partir des données observationnelles françaises.
À partir du registre de l’Assurance maladie et des codes diagnostiques d’hospitalisation, les données des enfants de moins de 3 ans ayant eu au moins une délivrance du médicament entre juillet 2014 et juin 2016 ont été retrouvées. L’analyse concernaient 1 484 enfants “sains” c’est-à-dire sans pathologie cardiaque, respiratoire ou métabolique associées à l’hémangiome et 269 enfants avec au moins une de ces 3 complications.
Sur les 1 753 enfants inclus, 23,9 % étaient nés prématurément. Avant le traitement par propranolol oral, 6,2 % avaient reçu du timolol ophtalmique et 16 % des corticoïdes systémiques. L’âge moyen de début du traitement était de 5,7 mois [0-35] et l’âge médian de 4 mois. La plupart des enfants ne recevaient qu’une seule cure de médicament avec une durée médiane de 5,4 mois [3,2-7,5]. Au cours de la période d’exposition, 2 enfants sains ont eu une complication cardiovasculaire (une hypotension et une bradycardie) ayant conduit à une suspension du traitement quelques mois. Sur le plan respiratoire, 51 événements respiratoires aigus étaient notés, il existait un risque significativement augmenté d’hospitalisation pour bronchiolite en cas de traitement par rapport à la population non traitée avec un indice standardisé de morbidité (ISM) de 1,6 [IC 95 % : 1,1-2,1]. Sur le plan métabolique, 3 hypoglycémies étaient observées sans risque relatif identifié. Chez les enfants ayant des pathologies associées, parmi les 133 ayant une cardiopathie[...]
Connectez-vous pour consulter l'article dans son intégralité.
Vous êtes abonné(e)
IDENTIFIEZ-VOUS
Pas encore abonné(e)
INSCRIVEZ-VOUS
Inscrivez-vous gratuitement et profitez de tous les sites du groupe Performances Médicales
S'inscrire