Quoi de neuf en pneumologie pédiatrique ?
À la question “quoi de neuf mamie ?”, ma grand-mère répondait…

À la question “quoi de neuf mamie ?”, ma grand-mère répondait…
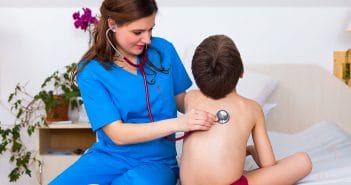
La dyspnée est définie comme une “expérience subjective d’inconfort respiratoire qui se manifeste par des sensations qualitativement différentes, variant en intensité” ; sa physiopathologie n’est pas claire. C’est une plainte fréquente en consultation de pédiatrie, surtout la dyspnée d’effort. Le 1er diagnostic évoqué lors d’une gene respiratoire à l’effort est souvent celui d’asthme d’effort, mais il existe de nombreuses autres causes qu’il ne faut pas méconnaître. Pour cela, une anamnèse complète est nécessaire, complétée par deux examens complémentaires de 1re intention : la radiographie de thorax et l’EFR. En l’absence d’étiologie organique évidente, et lorsque la radio et les EFR sont normales, une épreuve d’effort est indiquée afin d’évaluer quelle est la dyspnée induite et l’adaptation cardiorespiratoire à l’effort.
Finalement, le diagnostic le plus fréquent, lorsque les bêta 2 mimétiques ne sont pas efficaces, est une limitation à l’effort physiologique.

Franklin D et al. A randomized trial of high-flow oxygen…
Jackson DJ et al. Quintupling inhaled glucocorticoids to prevent childhood…

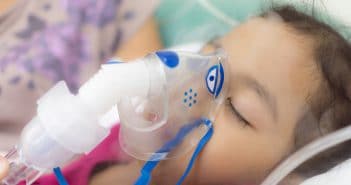
Au cours de la première année de vie, un enfant sur deux présente des épisodes de sifflements respiratoires (wheezing), mais seuls 20 % continueront à siffler par la suite. De nombreuses études, en particulier l’étude ISAAC (International Study of Asthma and Allergies in Childhood) déclinée en plusieurs phases, indiquent que la prévalence cumulée de l’asthme se situe autour de 9-10 % en France. Les asthmologues pensent que l’asthme n’est pas une “maladie autonome” mais un syndrome – “le syndrome asthmatique” – englobant plusieurs affections (endotypes) ayant des mécanismes physiopathologiques particuliers et des associations à facteurs environnementaux et génétiques. Toutefois, ces endotypes sont encore mal définis et les spécialistes recherchent plutôt des phénotypes particuliers dont l’identification pourrait déboucher sur des traitements mieux ciblés.
Les symptômes d’asthme varient spontanément avec le temps chez le même patient. Sauf cas d’espèce, il est recommandé de ne pas évaluer la sévérité de l’asthme sur une seule estimation.
Le diagnostic de l’asthme repose sur des critères simples et précis, cliniques et biologiques, que l’on peut réunir dans un “index de prédiction de l’asthme” (API). L’API doit ainsi permettre d’éviter tout à la fois le “sur-diagnostic” de l’asthme mais le “sous-diagnostic” est au moins aussi important.
Doyle L et al. Ventilation in extremely preterm infants and…
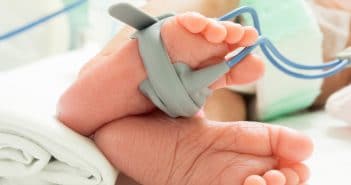
La saturation pulsée en oxygène (SpO2) est un paramètre vital facilement et rapidement mesurable, quel que soit l’âge du patient pédiatrique. Néanmoins, comme tout paramètre, sa mesure doit être réalisée dans des conditions optimales afin d’éviter des erreurs d’interprétation et de surcroît des erreurs diagnostiques et thérapeutiques.
Après quelques rappels sur le principe de mesure de la SpO2, nous allons tenter de répertorier les principaux facteurs pouvant être à l’origine d’un risque d’erreur. Nous proposons ensuite un algorithme décisionnel (d’après Verhovsek et al.) face à une désaturation afin d’aider le praticien dans sa démarche diagnostique et, si confirmation de l’hypoxémie, nous rappelons les objectifs de SpO2 proposés en 2012 par le Groupe de Recherche sur les Avancées en Pneumologie Pédiatriques (GRAPP), en fonction de la situation clinique.
L’asthme et l’allergie alimentaire (AA) sont deux pathologies qui interfèrent de façon très étroite. La perception par les asthmatiques du rôle des aliments comme déclencheurs de leurs crises est élevée. Les études précises, basées en particulier sur les tests de provocation par voie orale montrent que l’AA peut être est la cause d’un asthme dans moins de 6 % des cas. Par contre, la fréquence de l’AA associée à l’asthme est plus importante, autour de 20 % des cas. Il faut penser à une AA devant tout asthme non amélioré par un traitement correct, s’il existe des symptômes extra-respiratoires (urticaire, symptômes digestifs, eczéma, allergies multiples) et si le patient est fortement atopique.
La présence d’une IgE-réactivité isolée (PT et/ou dosages d’IgEs positifs) est fréquente, sans valeur diagnostique pour l’AA. L’AA est un facteur de risque d’asthme aigu grave. Inversement, l’asthme est un facteur de risque d’AA grave pouvant mettre la vie en jeu. Parmi les facteurs de risque d’AA potentiellement mortelle, il faut insister sur la présence d’un asthme sous-jacent et la sous-utilisation de l’adrénaline, victime d’un ostracisme persistant malgré les recommandations régulièrement émises.
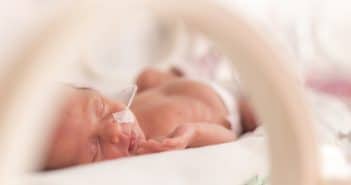
Les conséquences respiratoires de la prématurité ne sont pas limitées à la période néonatale et la naissance prématurée est associée à une morbidité respiratoire tout au long de la vie, même en l’absence de maladie respiratoire néonatale. L’impact clinique est essentiellement représenté par une augmentation de la fréquence de l’asthme et, dans une moindre mesure, d’une moins bonne tolérance à l’effort. L’impact fonctionnel correspond surtout à des valeurs de VEMS un peu abaissées. Enfin, la persistance d’anomalies radiologiques est également bien décrite. Les mécanismes en cause dans l’ensemble de ces processus sont encore incomplètement connus. Un calibre réduit des voies aériennes, mais aussi des phénomènes inflammatoires actifs persistants et une sénescence cellulaire accélérée pourraient être à l’origine des complications observées.

Le microbiome respiratoire est une entité mise en évidence grâce à l’avènement des techniques de biologie moléculaire. Ce microbiote existe probablement déjà in utero pour se modifier au cours de la croissance. Il interagit avec le microbiote digestif mais également avec le microbiote cutané et l’oropharynx. Les études dans le modèle murin nous montre qu’il existe une interaction entre le microbiote digestif et pulmonaire. Cette interaction intervient dans l’immunité pulmonaire innée et la modification de la réponse inflammatoire. Les comparaisons du microbiote chez l’enfant et l’adulte “sain” et asthmatique montrent qu’il existe une différence entre ces deux populations. Cette différence pourrait intervenir dans la genèse de l’asthme ou favoriser une réponse au traitement inhalé différente.
